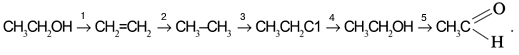|
|
МЕНЮ
|
Курсовая работа: Методические разработки урока по теме "Спирты"Гидролиз древесины — каталитический процесс взаимодействия полисахаридов (целлюлозы, пентозанов и гексозанов гемицеллюлоз) с водой. При этом они превращаются в соответствующие моносахариды: ксилозу, a-D-глюкозу и т. д., например:
Катализаторы процесса гидролиза —концентрированные и разбавленные кислоты или кислые соли. При этом скорость гидролиза возрастает с увеличением константы диссоциации кислоты, ее концентрации и при повышении температуры гидролизата существенно зависят от природы катализатора. Гидролиз в присутствии разбавленной серной кислоты (0,4—0,7 %-ной) проводят при температуре 120—190 "С и давлении 0,6—1,2 МПа. В результате получают гидролизат, загрязненный фурфуролом, органическими кислотами и другими веществами. Это объясняется тем, что параллельно с гидролизом протекают реакции разложения образовавшихся моносахаридов, скорость которых с повышением температуры также возрастает. Поэтому, несмотря на то что константа скорости реакции гидролиза больше константы скорости реакции разложения, выход гексоз в этом Случае не превышает 70 % от теоретически возможного при степени гидролиза около 90%. Гидролиз в присутствии концентрированных кислот (70— 80 %-ной серной кислоты или 31—41 %-ной соляной кислоты) проводят при температуре не выше 60 "С и атмосферном давлении. Он дает чистый гидролизат с выходом моносахаридов до 95% от теоретически возможного. Брожение (ферментация) процесс разложения углеводов под воздействием микроорганизмов или выделенных из них ферментов. В производстве этанола используют одну из разновидностей брожения — спиртовое брожение, вызываемое ферментом зимазой, содержащимся в дрожжевых клетках. Из моносахаридов спиртовому брожению подвергаются только гексозы. Процесс спиртового брожения, a-D-глюкозы, составляющей структурную единицу целлюлозы, происходит без доступа кислорода (анаэробное брожение) и включает ряд стадий с участием фосфорорганических соединений. В результате сложных превращений из глюкозы образуется этанол. Параметры процесса брожения выбирают, исходя из оптимальных условий развития дрожжевых клеток и подавления развития их спутников — кислотообразующих бактерий молочнокислого и уксуснокислого брожения.
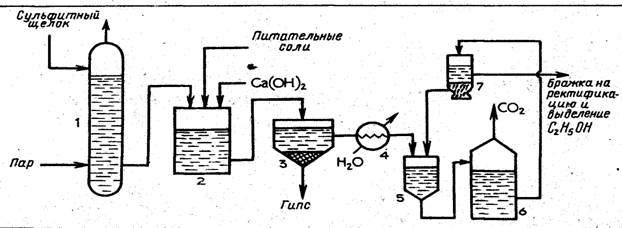
Так как оптимальные температуры размножения дрожжевых клеток практически совпадают и равны 35— 50 °С, то подавить развитие бактерий изменением температуры нельзя. Для этого повышают кислотность среды, вводя в гидролизат серную или молочную кислоту. При рН 4,2 дрожжевые клетки интенсивно растут, а бактерии не размножаются. Поэтому на практике процесс брожения проводят при температуре 27 С, атмосферном давлении и в кислой среде (рН= =3,8—4,0). Технологическая схема производства этанола гидролизом древесины. Процесс производства этанола складывается из двух последовательных стадий; объединенных в единую технологическую схему: гидролиза древесины и сбраживания образующегося гидролизата. В нашей стране распространен метод гидролиза древесины разбавленной серной кислотой. В качестве сырья используют отходы хвойной древесины с высоким содержанием гексозанов. Производство этанола по этой схеме представляет собой полунепрерывный перколяциоиный процесс, в основе которого лежит принцип: непрерывной фильтрации раствора кислоты через периодически загружаемое в реактор древесное сырье с непрерывным в течение нескольких часов отбором гидролизата.. При этом раствор кислоты служит одновременно экстрагентом образующихся при гидролизе моносахаридов. Схема производства этанола гидролизом древесины приведена на рис. 2. Древесное сырье в виде опилок или измельченной щепы загружают в гидролиз-аппарат 1 — цилиндрический стальной сосуд, футерованный внутри кислотоупорным материалом. После загрузки сырья в аппарат через специальное оросительное устройство подают нагретый до 1$0—190 °С раствор серной кислоты концентрацией около 0,5 %. Воду для получения раствора кислоты подогревают в подогревателе 2. В гидролиз-аппарат вводят также пар и создают давление 1,0—1,2 МПа. Через фильтрующее устройство, расположенное в нижней части гидролиз-аппарата и выполненное в виде перфорированных медных трубок, из аппарата непрерывно отводят гидролизат и направляют его в испаритель 4. Вследствие снижения давления гидролизат вскипает и пары, содержащие фурфурол (tKHn= 161,7 °С при атмосферном давлении), поступают в конденсатор 5. Цикл непрерывной работы гидролиз-аппарата от загрузки до выгрузки составляет несколько часов, затем оставшийся в нем лигнин передавливают после открытия заслонки в сборник после этого в аппарат загружают новую порцию древесного сырья. После отделения фурфурола гидролизат из испарителя поступает в нейтрализатор 6, куда подают раствор гидроксида кальция, а оттуда —
Сульфитный щелок подают в колонну /, где из него паром выдувают примеси. Очищенный щелок поступает в нейтрализатор 2, куда подают раствор гидроксида кальция и вводят питательные соли. Из нейтрализатора щелок после охлаждения до 30 °С в холодильнике 4 направляют сначала на первую ступень брожения в дрожжанку 5, а затем на вторую ступень брожения в бродильный чан 6 и в. сепаратор 7. В сепараторе дрожжи отделяются от образовавшейся бражки, и их возвращают в дрожжанку. После сепаратора бражку, содержащую 1,0— 1,2 % спирта, направляют на концентрирование и выделение этанола аналогично тому, как это происходит в производстве гидролизного этанола (см. рис. 2). Переработкой сульфитных щелоков можно получить (в расчете на 1 т воздушно-сухой древесины) 90—110 л этанола, 40—50 кг белковых дрожжей, 600—700 кг сухих лигносульфонатов. Комплексная переработка сульфитных щелоков имеет и большое значение в экологическом плане. Существующие промышленные способы производства целлюлозы не обеспечивают полной утилизации и переработки его отходов — варочных сульфитных щелоков и отдувочных газов. Вследствие этого целлюлозно-бумажная промышленность в настоящее время — одна из основных источников загрязнения водоемов сточными водами. этанол урок одноатомный спиртГлава 3. МЕТОДИЧЕСКИЕ РАЗРАБОТКИ ПО ТЕМЕ «СПИРТЫ»Система уроков по теме: "Предельные одноатомные спирты"Пояснительная записка. Все классы органических соединений преподаю блоками. Блок состоит из трех частей: 1. урок-лекция, 2. тренировочные домашние упражнения, 3. урок-коррекция. Урок-лекция (объяснение нового материала). Цели: - ввести понятие предельных одноатомных спиртов, свойств; - развитие интереса, умения выделять главное, научить сравнивать и анализировать. 1. Определение. Органические соединения, которые состоят из предельного углеводородного радикала и содержат одну функциональную гидроксильную группу (-ОН), называются насыщенными одноатомными спиртами. Общая
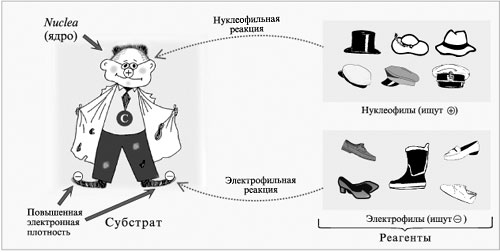
формула СnН2n+1ОН ( где n 2. Гомологический ряд и номенклатура СН3 ОН – метиловый спирт (метанол), СН3 СН2ОН – этиловый спирт (этанол)…. - СН2 - гомологическая разница Пример: 3-метилгексанол – 1 2. Изомерия положения функциональной группы (-ОН) Пример: бутанол-1 -> бутанол-2 3. Изомерия между классами (предельные одноатомные спирты изомерны простым эфирам) 4. Физические свойства 1) Спирты от С1 до С11 – жидкости, от С12 до С - твердые. 2) Легче воды, бесцветны, жидкие имеют резкий запах, твердые запаха не имеют. 3) Низшие спирты (до пропилового) смешиваются с водой в любых отношениях. Высшие спирты практически нерастворимы в воде. Межмолекулярная водородная связь возможна между отдельными молекулами спирта и между молекулами спирта и воды. Это влияет на физические свойства спиртов: повышает температуру кипения, снижает летучесть, способствует хорошей растворимости в воде, не позволяет перегонкой получить 100% спирт из его водного раствора.
5. Химические свойства (с примерами): 1) горение, 2) взаимодействие с активными металлами; 3) взаимодействие с органическими кислотами, с неорганическими кислотами; 4) с галогеноводородами; 5) окисление - первичный спирт -> альдегид, - вторичный спирт -> кетон, - третичный спирт: тяжело окисляется с разрывом С-С связи; 6) дегидратация: - внутримолекулярная, - межмолекулярная с образованием простых эфиров; 7) дегидратация и дегидрирование (реакция Лебедева). 6. Получение одноатомных спиртов (с примерами). В промышленности: 1) получение СН3 ОН - из синтез-газа - во время сухой перегонки древесины (древесный спирт), 2) гидратация алкенов, 3) брожение сахаристых веществ. В лаборатории: 1) из алканов через галогенопроизводные, 2) восстановление альдегидов. Физиологическое действие спиртов на организм негативно. СН3 ОН – сильный яд! В малых количествах вызывает слепоту, в больших – приводит к смерти. С2Н5ОН – наркотик. Под влиянием этанола у человека ослабляется внимание, затормаживается реакция, нарушается корреляция движений. При продолжительном употреблении вызывает глубокие нарушения нервной системы, заболевания сердечно-сосудистой системы, пищеварительного тракта, наступает тяжелая болезнь – алкоголизм. 7. Применение спиртов. 1) Метанол: - в промышленном органическом синтезе (производство формальдегида), - как растворитель, - как добавка к бензину. 2) Этанол: - производство уксусной кислоты, - как растворитель, - в парфюмерии, - в медицине, - как топливо, - в пищевой промышленности. 8. Связь между ациклическими углеводородами и спиртами (показать на примерах). Домашнее задание: пар. 17 (учебник О.С. Габриелян), тренировочные упражнения. Приложение 1. Закрепление (если позволяет время) 1. Назвать по международной номенклатуре (2-4 примера). 2. Написать структурные формулы изомерных спиртов С4Н9 ОН и назвать их. Приложение 2. Тренировочные домашние упражнения. Тема: “Одноатомные спирты”. Сложность 1 (оценка “удовлетворительно”). 1. Написать структурные формулы следующих соединений: 2-метилпентанол-1; 2,3-диметилбутанол-2; 2-метилпентен-1-ол-3. 2. Назвать вещество и написать два его гомолога и два изомера
1. Какой объем водорода выделится при взаимодействии 19,5 г калия с этанолом. Сложность 2 (оценка “хорошо”). 1. Чем объясняется изомерия спиртов? Пояснить это на примере спирта, в молекуле которого четыре атома углерода. Назвать каждый изомер. 2. Написать реакции получения метанола. 3. Осуществить превращения: Этан -> бромэтан-> этен-> этанол-> метилэтиловый эфир. Где происходит дегиратация? 4. При сжигании 4,8 г органического вещества образовалось 3,36 л оксида углерода (IV) и 5,4 г воды. Плотность паров этого вещества по метану 2. Определить формулу вещества. Сложность 3 (оценка “отлично”). 1. Чем отличаются первичные, вторичные и третичные спирты? (Привести примеры каждого и назвать их) 2. Предложить схему получения из пропана пропанол-1. 3. Осуществить превращения (предложить две цепочки). 4. При межмолекулярной дегидратации 100г одноатомного предельного спирта неизвестного строения выделилось 21,09 г воды и выход продукта реакции составил 75% от теоретического. Определить строение спирта. Урок-коррекция. 1 этап. 10-15 минут. Учащиеся задают вопросы по тренировочным упражнениям. 2 этап. 20-30 минут. Самостоятельная работа. Работа разноуровневая. Учащиеся выбирают любой вариант. Самостоятельная работа (тема: “Одноатомные спирты”). Оценка “удовлетворительно”
Оценка “хорошо”
Оценка “отлично”
Химические свойства спиртовОдноатомные спирты не обладают ни щелочными, ни кислотными свойствами. Водные растворы спиртов на индикаторы не действуют. Рассмотрим химические свойства спиртов на примере этанола. В молекуле этилового спирта СН3–СН2–ОН имеется четыре типа химических связей, различающихся полярностью: 1) Н–О; 2) С–О; 3) С–Н; 4) С–С. В результате химических превращений разрываются наиболее полярные связи Н–О, С–О и С–Н. Неполярная связь С–С в реакциях спиртов не разрывается. 1. Разрыв связи Н–О в реакции с натрием:
2. Одновременный разрыв связей Н–О и С–Н, находящихся при спиртовом атоме углерода, под действием окислителя (CuO) с отщеплением молекулы Н2О и образованием альдегида (СН3СНО):
2.
Разрыв
связи 3. а) Действие кислот НСl или НВr с образованием галогеналканов:
б) Действие кислородсодержащих кислот – неорганических и органических – с образованием сложных эфиров (подробнее см. урок 29):
Модель нуклеофильного и электрофильного процессов
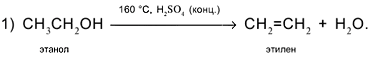
4. Внутримолекулярное отщепление Н и ОН от соседних атомов С в присутствии концентрированной серной кислоты при нагревании с образованием алкена:
5. Межмолекулярное отщепление Н и ОН от двух разных молекул спирта при умеренном нагревании в присутствии дегидратирующих агентов. Продукт реакции – простой эфир:
6. Спирты горят на воздухе с расщеплением всех связей и образованием углекислого газа и воды: С2Н5ОН
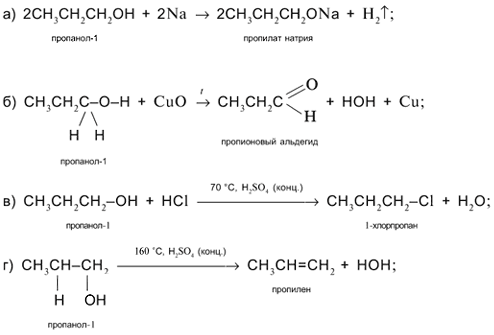
+ 3О2 Задача. Составьте уравнения реакций пропанола-1 СН3СН2СН2ОН со следующими реагентами: а) Na; б) CuO; в) HCl в присутствии H2SO4 (конц.) при нагревании; г) H2SO4 (конц.) при 160 °С (продукт – алкен); д) H2SO4 (конц.) при 140 °С (продукт – простой эфир). Решение
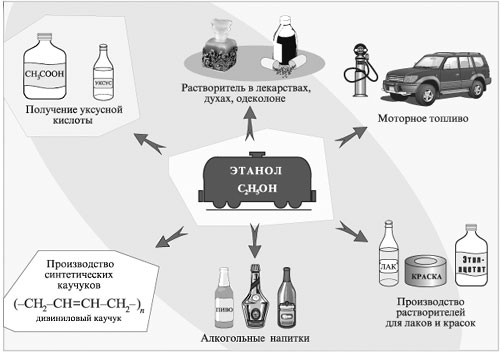
1. Составьте уравнения реакций пропанола-2 СН3СН(ОН)СН3 со следующими реагентами: а) Na; б) CuO; в) HCl в присутствии H2SO4 (конц.) при нагревании; г) H2SO4 (конц.) при 160 °С (продукт – алкен); д) H2SO4 (конц.) при 140 °С (продукт – простой эфир). 2. Алюминий реагирует со спиртами подобно натрию. При этом происходит замещение гидроксильного водорода на металл и выделение свободного водорода Н2. Реакция протекает при нагревании около температуры кипения спирта. Составьте уравнения реакций металлического алюминия со спиртами: а) метанолом; б) этанолом. 3. Почему температуры кипения спиртов выше, чем у соответствующих по молекулярной массе углеводородов (С2Н5ОН, Мr = 46, tкип = 78 °С; С3Н8, Мr = 44, tкип = –42 °С)? 4. Напишите схему реакций, с помощью которых пропанол-1 можно превратить в пропанол-2. Из спиртов ROH получают соединения многих других классов: алкилгалогениды RHal, алкены R'СН=СН2, простые эфиры RОR', сложные эфиры R'СООR, альдегиды R'СНО, карбоновые кислоты R'СООН и т.д. Спирты используют в качестве растворителей при синтезе новых соединений, производстве лаков и красок, фармацевтических препаратов, душистых веществ, парфюмерно-косметической продукции. Этанол используют как дезинфицирующее средство, горючее в двигателях. Он идет также на изготовление алкогольных напитков.
Применение этилового спирта Для прочного усвоения знаний по химии надо овладеть умением составлять и решать цепочки химических превращений. Решить цепочку – это значит записать уравнения реакций, соответствующие каждой стрелке схемы. В результате удается из имеющихся в наличии веществ получать новые необходимые вещества. Для решения цепочек необходимо знать: а) способы получения веществ и б) химические свойства веществ различных классов.
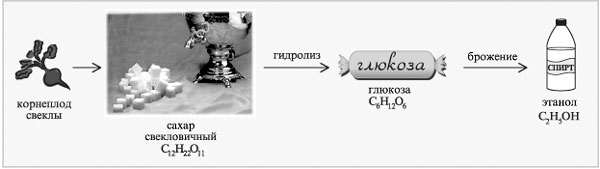
Пример цепочки химических превращений в производстве этанола
Задача. Составьте уравнения реакций для цепочки превращений:
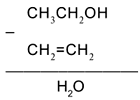
Решение Воспользуемся удобным способом, помогающим определять реагенты, требуемые для превращения одного вещества в другое: будем находить отличие в составе двух веществ, стоящих по разные стороны от стрелки, и из химической формулы с большим числом атомов вычитать формулу с меньшим числом атомов. Так, для первой стрелки схемы:
Следовательно, чтобы превратить спирт СН3СН2ОН в алкен СН2=СН2, надо отщепить молекулу воды от молекулы спирта:
Вторая реакция схемы состоит в присоединении водорода к алкену:
Третья стрелка схемы представляет реакцию замещения водорода в алкане СН3–СН3 на хлор. Это достигается действием молекулярного хлора на алкан:
Четвертое превращение – замещение атома хлора в хлорэтане С2Н5Сl на гидроксильную группу ОН:
Пятая реакция заключается в отщеплении двух атомов водорода от молекулы спирта. На практике это означает окисление спирта кислородом [O] окислителя, т.е. связывание избыточных атомов Н в форме Н2О:
ЛИТЕРАТУРА 1. О.В. Байдалина. О прикладном аспекте химических знании // Химия в школе, 2005, № 5, с. 45-47. 2. Ахметов Н.С. Методика преподавания темы «Закономерности протекания химических реакций» // Химия в школе. 2002, № 3, с. 15 – 18. 3. Ахметов Н.С. Учебник для 8 класса общеобразовательных учреждений. М.: Просвещение, 1998 г. 4. Рудзитис Г.Е., Фельдман Р.Г. Учебник для 8 класса средней школы. М.: Просвещение, 1992. 5. Материалы сайта www.1september.ru 6. О.С. Габриелян, Н.П. Воскобойникова, А. В. Ящукова. Настольная книга учителя. Химия. 8 класс. М.: Дрофа, 2003 г. 7. Малинин К.М. Технология серной кислоты и серы. М., Л., 1994. 8. Васильев Б.Г., Отвагина М.И. Технология серной кислоты. М., 1985. 9. Отвагина М.И., Явор В.И., Сретенская Н.С., Шарифов М.Ю. Промышленность минеральных удобрений и серной кислоты. М., НИИТЭХИМ. 1972. Выпуск № 4. 10. Резницкий И.Г. Возможности использования нитрозного способа для переработки газов автогенных процессов на серную кислоту / Цветные металлы. 1991. № 4. 11. Березина Л.Т., Борисова С.И. Утилизация фосфогипсов - важнейшая экологическая проблема // Химическая промышленность. 1999 г. № 12. 12. Громов А.П. Экологические аспекты производства серной кислоты // Экология и промышленность России. 2001, № 12. 13. Лидин Р.А. Химия: Руководство к экзаменам / Р. А. Лидин, В. Б. Маргулис. – М.: ООО Издательство «АСТ»: ООО «Издательство Астрель», 2003. с. 64 – 70. 14. Единый государственный экзамен 2002: Контрольные измерительные материалы: Химия / А.А. Каверина, Д.Ю. Добротин, М.Г. Снастина и др.; М.: Просвещение, 2002. – с. 39 – 51. 15. Химия: Большой справочник для школьников и поступающих в вузы / Е.А. Алферова, Н.С. Ахметов, Н.В. Богомолова и др. М.: Дрофа, 1999. с. 430-438 16. Р.П. Суровцева, С.В. Сафронов. Задания для самостоятельной работы по химии. М.: Просвещение, 1993 г. |
Страницы: 1, 2