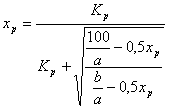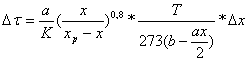|
|
МЕНЮ
|
Реферат: Производство серной кислоты5. Для получения улучшенной серной кислоты (содержание окислов азота N2O3 менее 0,5 ppm) предусмотрена схема подачи гидразингидрата в поток серной кислоты, поступающей на участок концентрирования серной кислоты. Гидразинсульфат, полученный при добавлении гидразина к серной кислоте, взаимодействует с нитрозилсернистой кислотой, обуславливающей содержание N2О3 в продуктовой кислоте:
Избыток гидразина окисляется с образованием элементарного азота:
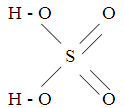
Химический состав серной кислоты выражается формулой H2SO4. Структурная формула серной кислоты выглядит следующим образом:
Относительная молекулярная масса серной кислоты - 98,08 кг/кмоль. Безводная серная кислота содержит 100 % H2SO4 или 81,63 % SO3 и 18,37 % мас. H2O. Это бесцветная маслянистая жидкость не имеющая запаха с температурой кристаллизации 10,37 ºС. Температура кипения безводной серной кислоты при давлении 1,01·105 Па (760 мм рт.ст.) составляет 298,2 ºС. Плотность при 20 ºС составляет 1830,5 кг/м3. С водой и сернистым ангидридом серная кислота смешивается в любых пропорциях. В процессе производства серной кислоты для окисления сернистого ангидрида в серный применяются ванадиевый катализатор. Он представляет собой пористое вещество, на которое нанесено активное комплексное соединение, содержащее пятиокись ванадия V2O5. В данном случае применяется катализатор марки VK-WSA фирмы "Хальдор Топсе". Температура зажигания катализатора 400-430 ºС. При температуре выше 620 ºС активность катализатора быстро снижается, т.к. при этом распадается активный комплекс, содержащий пятиокись ванадия (V2O5), а также разрушается структура носителя, что приводит к разрушению катализатора и образованию пыли. Срок службы катализатора не менее 4 лет. 8. Термодинамический анализ Расчет теплового эффекта реакции окисления SO2 в SO3: 2SO2 + O2 = 2 SO3
Q=-ΔН=196,6 кДж Реакция экзотермическая – протекает с выделением тепла. ΔS= ΔG=ΔH-TΔS=-196,6-298*17,66=-5459,28 Энергия Гиббса значительно меньше нуля. Это значит, что реакция термодинамически возможна. Расчет теплового эффекта реакции конденсации SO3: SO3 + H2O = H2SO4
Q=-ΔН=174,26 кДж Реакция экзотермическая- протекает с выделением тепла. ΔS= ΔG=ΔH-TΔS=-174,26-298*-288,07=-86019,12 Энергия Гиббса значительно меньше нуля. Это значит, что реакция термодинамически возможна. Таблица 1 Значения термодинамических величин
Таблица 2 Значения Кр для реакции окисления SO2 при различных температурах
Вывод: реакция окисления SO2 наиболее полно протекает при невысоких температурах. Из этого следует, реакцию окисления SO2 целесообразно проводить при невысоких температурах. Повышение давления, по принципу Ле-Шателье, влияет положительно. 9. Кинетика процесса окисления диоксида серы Константа скорости реакции: определяется из уравнения Аррениуса. К=К0*е(-Еа/RT)=9,3*105*е(-79000/430*8,31)=0,13 Еа- энергия активации (79000Дж/моль) R- газовая постоянная (8,31) Е- температура К0 – предэкспоненциальный множитель (9,3*105сек) Расчет равновесной степени превращения
Таблица 3 Значения равновесной степени превращения при разных температурах
Таблица 4 Значения равновесной степени при различном содержании О2 и SO2 в газовой смеси
Исходя из полученных данных таблиц 3 и 4, можно сделать следующий вывод: с точки зрения равновесной степени превращения, процесс окисления диоксида серы нужно вести при низком содержании SO2 в газовой смеси и при низких температурах. Расчет времени контактирования газовой смеси в контактном аппарате Для того, чтобы рассчитать время контактирования, разделим слой катализатора на 5 частей.
Таблица 5 Время контактирования газа на первом слое катализатора
τ = ∑Δτ =3,188 сек Общее время контактирования на первом слое котализатораτ =3,188 сек. Таблица 5 Время контактирования газа на втором слое катализатора
τ = ∑Δτ =6,38 сек |
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.