|
|
МЕНЮ
|
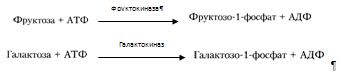
Курсовая работа: Анализ биохимических показателей работы печени в норме и патологииКурсовая работа: Анализ биохимических показателей работы печени в норме и патологииКУРСОВАЯ РАБОТА: АНАЛИЗ БИОХИМИЧЕСКИХ ПОКАЗАТЕЛЕЙ РАБОТЫ ПЕЧЕНИ В НОРМЕ И ПАТОЛОГИИ Cодержание Введение 1. Функциональная биохимия печени 1.1 Регуляторно–гомеостатическая функция печени 1.1.1 Углеводный обмен в печени и его регуляция 1.1.2 Регуляция липидного обмена 1.1.3 Регуляция обмена белков 1.1.4 Участие печени в обмене витаминов 1.1.5 Участие печени в водно-минеральном обмене 1.1.6 Участие печени в пигментном обмене 1.2 Мочевинообразовательная функция 1.3 Желчеобразовательная и экскреторная функция 1.4 Биотрансформационная (обезвреживающая) функция 2. Заболевания печени и лабораторная диагностика заболеваний печени 2.1 Основы клинической лабораторной диагностики заболеваний печени 2.2 Основные клинико-лабораторные синдромы при поражениях печени 2.2.1 Синдром цитолиза 2.2.3 Синдром гепатодепрессии (малой недостаточности печени) 2.2.4 Синдром воспаления 2.2.5 Синдром шунтирования печени 2.2.6 Синдром регенерации и опухлевого роста печени Заключение Список литературы Биохимия печени включает как протекание нормальных обменных процессов, так и нарушения метаболизма веществ с развитием патологии. Изучение всех аспектов биохимии печени позволит видеть картину нормально функционирующего органа и его участие в работе всего организма и поддержании гомеостаза. Так же при нормальной работе печени осуществляется интеграция всех основных обменов в организме, причем удается наблюдать начальные этапы метаболизма (например, при первичном всасывании веществ из кишечника) и конечные этапы с последующим выведением продуктов обмена из организма. При нарушениях работы печени происходит сдвиг метаболизма в определенную сторону, поэтому необходимо изучение патологических состояний органа для дальнейшей диагностики заболеваний. В настоящее время это особенно актуально, так как заболевания печени прогрессируют, а достаточно хороших методов лечения пока не существует. К таким заболеваниям в первую очередь относятся вирусные гепатиты, циррозы печени (часто при систематическом употреблении алкоголя и при прочих вредных внешних воздействиях, связанных с неблагоприятной экологией), сдвиги метаболизма при нерациональном питании, онкологические заболевания печени. Поэтому очень важна ранняя диагностика этих заболеваний, которая может основываться на биохимических показателях. Целью курсовой работы является рассмотрение функций печени и сравнение биохимических показателей работы этого органа в норме и патологии; также указание основных принципов лабораторной диагностики, краткое описание синдромов гепатитов различной этиологии и приведение примеров. 1. Функциональная биохимия печени Условно функции печени по биохимическим показателям можно разделить на: регуляторно-гомеостатическую функцию, включающую основные виды обмена (углеводный, липидный, белковый, обмен витаминов, водно-минеральный и пигментный обмены), мочевинообразовательную, желчеобразовательную и обезвреживающую функции. Такие основные функции и их регуляция подробно рассмотрены далее в этой главе. 1.1 Регуляторно–гомеостатическая функция печениПечень – центральный орган химического гомеостаза, где чрезвычайно интенсивно протекают все обменные процессы и где они тесно переплетаются между собой. 1.1.1 Углеводный обмен в печени и его регуляцияМоносахариды (в частности глюкоза) поступают в печень по воротной вене и подвергаются различным преобразованиям. Например, при избыточном поступлении глюкозы из кишечника она депонируется в виде гликогена, так же глюкоза производится печенью в ходе гликогенолиза и глюконеогенеза, поступает в кровь и расходуется большинством тканей. Регуляция углеводного обмена осуществляется благодаря тому, что печень является практически единственным органом, который поддерживает постоянный уровень глюкозы в крови даже в условиях голодания. Судьба моносахаридов различна в зависимости от природы, их содержания в общем кровотоке, потребностей организма. Часть их отправится в печёночную вену, чтобы поддержать гомеостаз, в первую очередь, глюкозы крови и обеспечить нужды органов. Концентрация глюкозы в крови определяется балансом скоростей ее поступления, с одной стороны, и потребления тканями с другой. В постабсорбтивном состоянии (постабсорбтивное состояние развивается через 1,5—2 часа после приема пищи, так же называется истинным или метаболическим насыщением [1]. Типичным постабсорбтивным состоянием считают состояние утром до завтрака, после примерно десятичасового ночного перерыва в приеме пищи) и в норме концентрация глюкозы в крови равна 60-100 мг/дл (3,3-5,5 моль\л). А остальную часть моносахаридов (в основном глюкозы) печень использует для собственных нужд. В гепатоцитах интенсивно протекает метаболизм глюкозы. Поступившая с пищей глюкоза только в печени с помощью специфических ферментных систем преобразуются в глюкозо-6-фосфат (лишь в такой форме глюкоза используется клетками) [6]. Фосфорилирование свободных моносахаридов – обязательная реакция на пути их использования, она приводит к образованию более реакционно-способных соединений и поэтому может рассматриваться как реакция активации. Галактоза и фруктоза, поступающие из кишечного тракта, при участии соответственно галактокиназы и фруктокиназы фосфорилируются по первому углеродному атому:
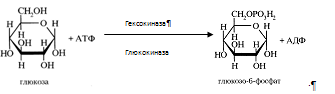
Глюкоза, поступающая в клетки печени, так же подвергается фосфорилированию с использованием АТФ. Эту реакцию катализирует ферменты гексокиназа и глюкокиназа. печень патология диагностика заболевание
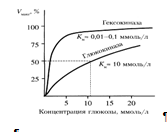
Гексокиназа обладает высоким сродством к глюкозе (Км <0,1 ммоль/л), поэтому максимум скорости реакции достигается при низкой концентрации глюкозы. Глюкозо-6-фосфат ингибирует гексокиназу. Глюкокиназа отличается от гексокиназы высоким значением Км для глюкозы – 10 ммоль/л и не ингибируется глюкозо-6-фосфатом. Это обеспечивает взаимное фунционирование обоих ферментов в печени. В постабсорбтивном состоянии концентрация глюкозы в крови низкая, около 5 ммоль/л и скорость глюкокиназной реакции примерно 1/5 от максимальной скорости. В таких условиях максимально работает гексокиназа. Во время пищеварения в воротную вену и далее в печень поступают большие количества глюкозы, и ее концентрация достигает и превышает 10 ммоль/л. Соответственно увеличивается скорость глюкокиназной реакции, причем если не происходит ингибирование гексокиназы глюкозо-6-фосфатом, то скорость гексокиназной реакции не падает. Что видно из графика:
Наряду с другими механизмами это предотвращает черезмерное повышение концентрации глюкозы в периферической крови при пищеварении [7]. Образование глюкозо-6-фосфата в клетке – своеобразная «ловушка» для глюкозы, так как мембрана клетки непроницаема для фосфорилированной глюкозы (нет соответствующих транспортных белков). Кроме того, фосфорилирование уменьшает концентрацию свободной глюкозы в цитоплазме. В результате создаются благоприятные условия для облегченной диффузии глюкозы в клетки печени из крови.
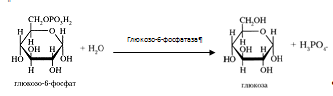
Возможна и обратная реакция превращения глюкозо-6-фосфат в глюкозу при действии глюкозо-6-фосфатазы, которая катализирует отщепление фосфатной группы гидролитическим путем. Образовавшаяся свободная глюкоза способна диффундировать из печени в кровь. В других органах и тканях (кроме почек и клеток кишечного эпителия) глюкозо-6-фосфатазы нет, и поэтому там проходит только фосфорилирование, без обратной реакции, и выход глюкозы из этих клеток невозможен [3].
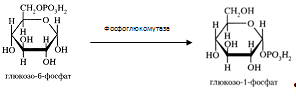
Глюкозо-6-фосфат может превратиться в глюкозо-1-фосфат при участии фосфоглюкомутазы, которая катализирует обратимую реакцию. Так же глюкозо-6-фосфат может использоваться в различных превращениях, основными из которых являются: синтез гликогена, катаболизм с образованием СО2 и Н2О или лактата, синтез пентоз. Вместе с тем в процессе метаболизма глюкозо-6-фосфата образуются промежуточные продукты, используемые в дальнейшем для синтеза аминокислот, нуклеотидов, глицерина и жирных кислот. Таким образом, глюкозо-6-фосфат – не только субстрат для окисления, но и строительный материал для синтеза новых соединений (приложение 1). Итак, рассмотрим окисление глюкозы и глюкозо-6-фосфата в печени. Этот процесс идет двумя путями: дихотомическим и апотомическим. Дихотомический путь это гликолиз, который включает «анаэробный гликолиз», завершающийся образованием молочной кислоты (лактата) или этанола и СО2 и «аэробный гликолиз» – распад глюкозы, проходящий через образование глюкозо-6-фосфата, фруктозобисфосфата и пирувата как в отсутствие так и в присутствие кислорода (аэробный метаболизм пирувата выходит за рамки углеводного обмена, однако может рассматриваться как завершающая его стадия: окисление продукта гликолиза – пирувата). Апотомический путь окисления глюкозы или пентозный цикл заключается в образовании пентоз и возвращению пентоз в гексозы в результате распадается одна молекула глюкозы и образуется СО2 . Гликолиз в анаэробных условиях - сложный ферментативный процесс распада глюкозы, протекающий без потребления кислорода. Конечным продуктом гликолиза является молочная кислота. В процессе гликолиза образуется АТФ. Процесс гликолиза протекает в гиалоплазме (цитозоле) клетки и условно делится на одиннадцать этапов, которые соответственно катализируют одиннадцать ферментов: 1. Фосфорилирование глюкозы и образование глюкозо-6-фосфата – перенос остатка ортофосфата на глюкозу за счет энергии АТФ. Катализатором является гексокиназа. Этот процесс был рассмотрен выше.
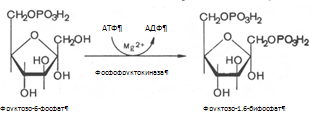
2. Превращение глюкозо-6-фосфата под действием фермента глюкозо-6-фосфат-изомеразы во фруктозо-6-фосфат: 3. Фруктозо-6-фосфат вновь фосфорилируется за счет второй молекулы АТФ, реакция катализируется фосфофруктокиназой:
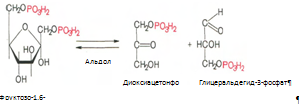
Реакция необратима, протекает в присутствии ионов магния и является наиболее медленно текущей реакцией гликолиза. 4. Под влиянием фермента альдолазы фруктозо-1,6-бифосфат расщепляется на две фосфотриозы:
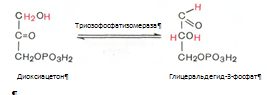
5. Реакция изомеризации триозофосфатов. Катализируеися ферментом триозофосфатизомеразой:
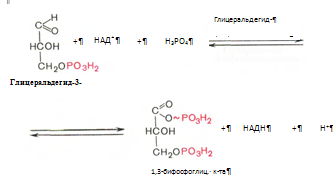
6. Глицеральдегид-3-фосфат в присутствии фермента глицеральдегидфосфатдегидрогеназы, кофермента НАД и неорганического фосфата продвергается своеобразному окислению с образованием 1,3-бифосфоглицериновой кислоты и восстановленой формы НАД – НАД*Н2 :
7. Реакция катализируется фосфоглицераткиназой, происходит передача фосфатной группы в положении 1 на АДФ с образованием АТФ и 3-фосфоглицериновой кислоты (3-фосфоглицерат):
8. Внутримолекулярный перенос оставшейся фосфатной группы, и 3-фосфоглицериновая кислота превращается в 2-фосфорлицериновую кислоту (2-фосфоглицерат):
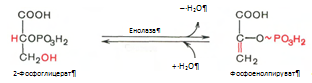
Реакция легкообратима и протекает в присутствии ионов магния. 9. Реакция катализируется ферментом енолазой, 2-фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват), а фосфатная связь в положении 2 становится макроэргической:
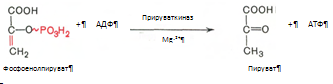
10. Разрыв макроэргической связи и перенос фосфатного остатка от фосфоенолпирувата на АДФ. Кртализируется ферментом пируваткиназой:
11. Восстановление пировиноградной кислоты и образование молочной кислоты (лактата). Реакция протекает при участии фермента лактатдегидрогеназы и кофермента НАД*Н2, образовавшегося в шестой ркакции:
Гликолиз в аэробных условиях. В этом процессе можно выделить три части: 1. специфические для глюкозы превращения, завершающиеся образованием пирувата (аэробный гликолиз); 2. общий путь катаболизма (окислительное декарбоксилирование пирувата и цитратный цикл); 3. митохондриальная цепь переноса электронов. В результате этих процессов глюкоза в печени распадается до С02 и Н20, а освобождающаяся энергия используется для синтеза АТФ (приложение 2). К обмену углеводов в печени относятся только специфические для глюкозы превращения, где происходит распад глюкозы до пирувата, который можно разделить на два этапа: 1. От глюкозы до глицеральдегидфосфата. В реакциях происходит включение фосфатных остатков в гексозы и превращение гексозы в триозу (приложение 3). Реакции этого этапа катализируют следующие ферменты: гексокиназа или глюкокиназа (1); фосфоглюкоизомераза (2); фосфофруктокиназа (3); альдолаза фруктозо-1,6-бисфосфата (4); фосфотриозоизомераза (5) 2. От глицеральдегидфосфата до пирувата. Это реакции, связанные с синтезом АТФ. Этап завершается превращением каждой молекулы глюкозы в две молекулы глицеральдегидфосфата (приложение 4). В реакциях участвуют пять ферментов: дегидрогеназа глицеральдегидфосфата (6); фосфоглицераткиназа (7); фосфоглицеромутаза (8); енолаза (9); пируваткиназа (10). Пентозофосфатный (фосфоглюконатный) путь превращения глюкозы обеспечивает клетку гидрированным НАДФ для восстановительных синтезов и пентозами для синтеза нуклеотидов. В пентозофосфатном пути можно выделить две части — окислительный и неокислительный пути. 1. Окислительный путь включает две реакции дегидрирования, где акцептором водорода служит НАДФ (приложение 5). Во второй реакции одновременно происходит декарбоксилирование, углеродная цепь укорачивается на один атом углерода и получаются пентозы. 2. Неокислительный путь значительно сложнее. Здесь нет реакций дегидрирования, он может служить только для полного распада пентоз (до С02 и Н20) или для превращения пентоз в глюкозу (приложение 6). Исходными веществами являются пять молекул фруктозо-6-фосфата, в сумме содержащие 30 углеродных атомов, конечный продукт реакции — шесть молекул рибозо-5-фосфата, в сумме также содержащие 30 углеродных атомов.
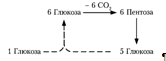
Окислительный путь образования пентоз и путь возращения пентоз в гексозы вместе составляют циклический процесс: В этом цикле за один оборот полностью распадается одна молекула глюкозы, все шесть углеродных атомов которой превращаются в С02 [7]. Так же в печени идет обратный гликолизу процесс – глюконеогенез. Глюконеогенез — процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Глюконеогенез обеспечивает синтез 80-100 г глюкозы в сутки. Первичные субстраты глюконеогенеза — лактат, аминокислоты и глицерол. Включение этих субстратов в глюконеогенез зависит от физиологического состояния организма. Лактат — продукт анаэробного гликолиза. Он образуется при любых состояниях организма в эритроцитах и работающих мышцах. Таким образом, лактат используется в глюконеогенезе постоянно. Глицерол высвобождается при гидролизе жиров в жировой ткани в период голодания или при длительной физической нагрузке. Аминокислоты образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе. Необходимо отметить, что гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях [3]. Глюконеогенез в основном протекает по тому же пути, что и гликолиз, но в обратном направлении (приложение 7). Однако три реакции гликолиза необратимы, и на этих стадиях реакции глюконеогенеза отличаются от реакций гликолиза.
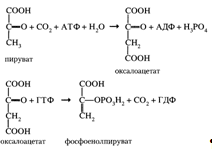
Превращение пирувата в фосфоенолпируват (необратимая стадия I) осуществляется при участии двух ферментов: пируваткарбоксилазы и карбоксикиназы фосфоенолпирувата:
Две другие необратимые стадии катализируются фосфатазой фруктозо-1,6-бисфосфата и фосфатазой глюкозо-6-фосфата: Каждая из необратимых реакций гликолиза вместе с соответствующей ей реакцией глюконеогенеза образует субстратный цикл (приложение 7, реакции 1, 2, 3). Синтез глюкозы (глюконеогенез из аминокислот и глицерина). Глюкоза в печени может синтезироваться из аминокислот и глицерина. При катаболизме аминокислот в качестве промежуточных продуктов образуются пируват или оксалоацетат, которые могут включаться в путь глюконеогенеза на стадии первого субстратного цикла (приложение 7, реакция 1). Глицерин образуется при гидролизе жиров и может превращаться в глюкозу (приложение 8). Аминокислоты и глицерин используются для синтеза глюкозы главным образом при голодании или при низком содержании углеводов в рационе (углеводное голодание). Глюконеогенез может так же происходить из лактата. Молочная кислота не является конечным продуктом обмена, но ее образование — это тупиковый путь метаболизма: единственный способ использования молочной кислоты связан с ее превращением вновь в пируват при участии той же лактатдегидрогеназы: |
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.