|
|
МЕНЮ
|
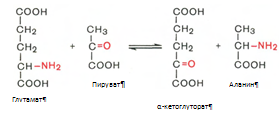
Курсовая работа: Анализ биохимических показателей работы печени в норме и патологииОбразование кетоновых тел происходит в несколько этапов (приложение 16). На первом этапе из 2 молекул ацетил-КоА образуется ацетоацетил-КоА. Реакция катализируется ферментом ацетил-КоА-ацетилтрансферазой (3-кетотиолазой). Затем ацетоацетил-КоА взаимодействует еще с одной молекулой ацетил-КоА. Реакция протекает под влиянием фермента гидроксиметилглутарил-КоА-синтетазы. Образовавшийся в-окси-в-метилглутарил-КоА способен под действием гидроксиметилглутарил-КоА-лиазы расщепляться на ацетоацетат и ацетил-КоА. Ацетоацетат восстанавливается при участии НАД-зависимой D-3-гидроксибутиратдегидрогеназы, при этом образуется D-в-оксимасляная кислота (D-3-гидроксибутират). Существует второй путь синтеза кетоновых тел. Образовавшийся путем конденсации 2 молекул ацетил-КоА ацетоацетил-КоА способен отщеплять коэнзим А и превращаться в ацетоацетат. Этот процесс катализируется ферментом ацетоацетил-КоА-гидролазой (деацилазой). Однако второй путь образования ацетоуксусной кислоты (ацетоацетата) не имеет существенного значения, так как активность деацилазы в печени низкая. В крови здорового человека кетоновые тела содержатся лишь в очень небольших концентрациях (в сыворотке крови 0,03–0,2 ммоль/л). Следует подчеркнуть важную роль кетоновых тел в поддержании энергетического баланса. Кетоновые тела – поставщики топлива для мышц, почек и действуют, возможно, как часть регуляторного механизма с обратной связью, предотвращая чрезвычайную мобилизацию жирных кислот из жировых депо. Печень в этом смысле является исключением, она не использует кетоновые тела в качестве энергетического материала. Из митохондрий печени эти соединения диффундируют в кровь и переносятся к периферическим тканям. Печень является центральным местом обмена ВЖК. Сюда они поступают из кишечника, жировых депо в составе альбуминов плазмы крови [5]. Регуляция синтеза и распада жиров в печени. В клетках печени есть активные ферментные системы и синтеза, и распада жиров. Регуляция обмена жиров в значительной мере определяется регуляцией обмена жирных кислот, но не исчерпывается этими механизмами. Синтез жирных кислот и жиров активируется при пищеварении, а их распад — в постабсорбтивном состоянии и при голодании. Кроме того, скорость использования жиров пропорциональна интенсивности мышечной работы. Регуляция обмена жиров тесно сопряжена с регуляцией обмена глюкозы. Как и в случае обмена глюкозы, в регуляции обмена жиров важную роль играют гормоны инсулин, глюкагон, адреналин и процессы переключения фосфорилирования-дефосфорилирования белков. Регуляция обмена белков в печени осуществляется благодаря интенсивному биосинтезу в ней белков и окислению аминокислот. За сутки в организме человека образуется около 80—100 г белка, из них половина в печени. При голодании печень быстрее всех расходует свои резервные белки для снабжения аминокислотами других тканей. Потери белка в печени составляют примерно 20%; в то время как в других органах не более 4%. Белки самой печени в норме обновляются полностью каждые 20 суток. Большинство синтезированных белков печень отправляет в плазму крови. При потребности (например, при полном или белковом голодании) эти протеины так же служат источниками необходимых аминокислот.Поступив через воротную вену в печень, аминокислоты подвергаются ряду превращений, так же значительная часть аминокислот разносится кровью по всему организму и используется для физиологических целей. Печень обеспечивает баланс свободных аминокислот организма путем синтеза заменимых аминокислот и перераспределения азота. Всосавшиеся аминокислоты в первую очередь используются в качестве строительного материала для синтеза специфических тканевых белков, ферментов, гормонов и других биологически активных соединений. Некоторое количество аминокислот подвергается распаду с образованием конечных продуктов белкового обмена (СО2, Н2О и NH3) и освобождением энергии. Все альбумины, 75-90% б-глобулинов (б1-антитрипсин, б2-макроглобулин – ингибиторы протеаз, белки острой фазы воспаления), 50% в-глобулинов плазмы синтезируются гепатоцитами. В печени происходит синтез белковых факторов свертывания крови (протромбина, фибриногена, проконвертина, акцелератора глобулина, фактора Кристмаса, фактора Стюарта-Прауэра) и часть естественных основных антикоагулянтов (антитромбин, протеин С и др.). Гепатоциты участвуют в образовании некоторых ингибиторов фибринолиза, регуляторы эритропоэза – эритропоэтины – образуются в печени. Гликопротеин гаптоглобин, вступающий в комплекс с гемоглобином для предупреждения его выделения почками, тоже имеет печёночное происхождение. Данное соединение принадлежит к белкам острой фазы воспаления, обладает пероксидазной активностью. Церулоплазмин, также являющийся гликопротеином, синтезируемым печенью, можно считать внеклеточной супероксиддисмутазой, что позволяет защищать мембраны клеток; мало того, он стимулирует продукцию антител. Подобным действием, только на клеточный иммунитет, обладает трансферрин, полимеризация которого так же осуществляется гепатоцитами. Ещё один углеводсодержащий белок, но с иммуносупрессивными свойствами, способен синтезироваться печенью – б-фетопротеин, рост концентрации которого в плазме крови служит ценным маркёром некоторых опухолей печени, яичек и яичников. Печень - источник большей части протеинов системы комплемента. В печени наиболее активно протекает обмен мономеров белков - аминокислот: синтез заменимых аминокислот, синтез небелковых азотистых соединений из аминокислот (креатина, глутатиона, никотиновой кислоты, пуринов и пиримидинов, порфиринов, дипептидов, коферментов пантотената и др.), окисление аминокислот с образованием аммиака, который обезвреживается в печени при синтезе мочевины [6]. Итак, рассмотрим общие пути обмена аминокислот. Общие пути превращения аминокислот в печени включают реакции дезаминирования, трансаминирования, декарбоксилирования и биосинтез аминокислот. Дезаминирование аминокислот. Доказано существование 4 типов дезаминирования аминокислот (отщепление аминогруппы) (приложение 17). Выделены соответствующие ферментные системы, катализирующие эти реакции, и идентифицированы продукты реакции. Во всех случаях NH2-группа аминокислоты освобождается в виде аммиака. Помимо аммиака, продуктами дезаминирования являются жирные кислоты, оксикислоты и кетокислоты. Трансаминирование аминокислот. Под трансаминированием подразумевают реакции межмолекулярного переноса аминогруппы (NH2—) от аминокислоты на б-кетокислоту без промежуточного образования аммиака. Реакции трансаминирования являются обратимыми и протекают при участии специфических ферментов аминотрансфераз, или трансаминаз. Пример реакции трансаминирования:
Декарбоксилирование аминокислот. Процесс отщепления карбоксильной группы аминокислот в виде СО2 . Образующиеся продукты реакции – биогенные амины. Реакции декарбоксилирования в отличие от других процессов промежуточного обмена аминокислот являются необратимыми. Они катализируются специфическими ферментами – декарбоксилазами аминокислот. Обезвреживание аммиака в организме. В организме человека подвергается распаду около 70 г аминокислот в сутки, при этом в результате реакций дезаминирования и окисления биогенных аминов освобождается большое количество аммиака, являющегося высокотоксичным соединением. Поэтому концентрация аммиака в организме должна сохраняться на низком уровне. Уровень аммиака в крови в норме не превышает 60 мкмоль/л . Аммиак должен подвергаться связыванию в печени с образованием нетоксичных соединений, легко выделяющихся с мочой. Один из путей связывания и обезвреживания аммиака в организме это биосинтез глутамина (и, возможно, аспарагина). Глутамин и аспарагин выделяются с мочой в небольшом количестве. Скорее они выполняют транспортную функцию переноса аммиака в нетоксичной форме. Синтеза глутамина, катализируется глутаминсинтетазой.
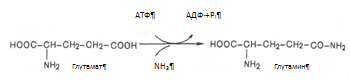
Второй и основной путь обезвреживания аммиака в печени – образование мочевины, который будет рассмотрен ниже в мочевинообразовательной функции печени. В гепатоцитах отдельные аминокислоты подвергаются специфическим преобразованиям. Из серосодержащих аминокислот образуется таурин, который позднее включается в парные жёлчные кислоты (таурохолевая, тауродезоксихолевая), а также может служить антиоксидантом, связывая гипохлорит анион, стабилизировать мембраны клеток; происходит активация метионина, который в виде S-аденозилметионина служит источником метильных групп реакциях окончания генеза креатина, синтеза холина для холинфосфатидов (липотропных веществ). Биосинтез заменимых аминокислот. Любая из заменимых аминокислот может синтезироваться в организме в необходимых количествах. При этом углеродная часть аминокислоты образуется из глюкозы, а аминогруппа вводится из других аминокислот путем трансаминирования. Алании, аспартат, глутамат образуются из пирувата, оксалоацетата и б-кетоглутарата соответственно. Глутамин образуется из глутаминовой кислоты при действии глутаминсинтетазы:
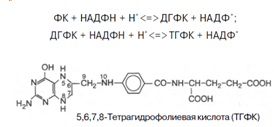
Аспарагин синтезируется из аспарагиновой кислоты и глутамина, который служит донором амидной группы; реакцию катализирует аспарагинсинтетаза пролин образуется из глутаминовой кислоты. Гистидин (частично заменимая аминокислота) синтезируется из АТФ и рибозы: пуриновая часть АТФ поставляет фрагмент —N=CH—NH— для имидазольного цикла гистидина; остальная часть молекулы образуется за счет рибозы. Если в пище нет заменимой аминокислоты, клетки синтезируют ее из других веществ, и тем самым поддерживается полный набор аминокислот, необходимый для синтеза белков. Если же отсутствует хотя бы одна из незаменимых аминокислот, то прекращается синтез белков. Это объясняется тем, что в состав подавляющего большинства белков входят все 20 аминокислот; следовательно, если нет хотя бы одной из них, синтез белков невозможен. Частично заменимые аминокислоты синтезируются в организме, однако скорость их синтеза недостаточна для обеспечения всей потребности организма в этих аминокислотах, особенно у детей. Условно заменимые аминокислоты могут синтезироваться из незаменимых: цистеин — из метионина, тирозин — из фенилаланина. Иначе говоря, цистеин и тирозин — это заменимые аминокислоты при условии достаточного поступления с пищей метионина и фенилаланина [5]. 1.1.4 Участие печени в обмене витаминовУчастие печени в обмене витаминов складывается из процессов депонирования всех жирорастворимых витаминов: А, Д, Е, К, F (секреция желчи так же обеспечивает всасывание этих витаминов) и многих из гидровитаминов (В12, фолиевая кислота, В1, В6, РР и др.), синтеза некоторых витаминов (никотиновая кислота) и коферментов. Особая печени заключается в том, что в ней происходит активация витаминов: 7. Фолиевая кислота с помощью витамина С восстанавливается в тетрагидрофолиевую кислоту (ТГФК) [8]; Восстановление сводится к разрыву двух двойных связей и присоединению четырех водородных атомов в положениях 5, 6, 7 и 8 с образованием тетрагидрофолиевой кислоты (ТГФК). Оно протекает в 2 стадии тканях при участии специфических ферментов, содержащих восстановленный НАДФ. Сначала при действии фолатредуктазы образуется дигидрофолиевая кислота (ДГФК), которая при участии второго фермента – дигидрофолатредуктазы – восстанавливается в ТГФК:
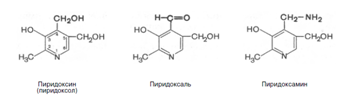
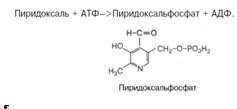
8. Витамины В1 и В6 фосфорилируются в тиаминдифосфат и пиридоксальфосфат соответственно [8]. Витамин В6 (пиридоксин) производный 3-оксипиридина. Термином витамин В6 обозначают все три производных 3-оксипиридина, обладающих одинаковой витаминной активностью: пиридоксин (пиридоксол), пиридоксаль и пиридоксамин:
Хотя все три производных 3-оксипиридина наделены витаминными свойствами, коферментные функции выполняют только фосфорилированные производные пиридоксаля и пиридоксамина. Фосфорилирование пиридоксаля и пиридоксамина является ферментативной реакцией, протекающей при участии специфических киназ. Синтез пиридоксальфосфата, например, катализирует пиридоксалькиназа:
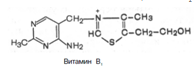
Витамин В1(тиамин). В химической структуре его содержатся два кольца – пиримидиновое и тиазоловое, соединенных метиленовой связью. Обе кольцевые системы синтезируются отдельно в виде фосфорилированных форм, затем объединяются через четвертичный атом азота. В превращении витамина B1 в его активную форму – тиаминпирофосфат (ТПФ), называемый также тиаминдифосфатом (ТДФ), участвует специфический АТФ-зависимый фермент тиаминпирофосфокиназа.
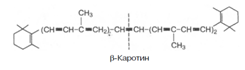
9. Часть каротинов преобразуется в витамин А под влиянием каротиндиоксигеназы. Каротины являются провитаминами для витамина А. Известны 3 типа каротинов: б-, в- и г-каротины, отличающиеся друг от друга химическим строением и биологической активностью. Наибольшей биологической активностью обладает в-каротин, поскольку он содержит два в-иононовых кольца и при распаде в организме из него образуются две молекулы витамина А:
При окислительном распаде б- и г-каротинов образуется только по одной молекуле витамина А, поскольку эти провитамины содержат по одному в-иононовому кольцу. 4. Витамин Д подвергается первому гидроксилированию на пути получения гормона кальцитриола; в печени осуществляется гидроксилирование в 25-м положении. Ферменты, катализирующие эти реакции, называются гидроксилазами, или монооксигеназами. В реакциях гидроксилирования используется молекулярный кислород. 5. Окислившийся витамин С восстанавливается в аскорбиновую кислоту; 6. Витамины РР, В2, пантотеновая кислота включаются в соответствующие нуклеотиды (НАД+, НАД+Ф, ФМН, ФАД, КоА-SH); 7. Витамин К окисляется, чтобы в виде своего пероксида служить коферментом в созревании (посттрансляционной модификации) белковых факторов свёртывания крови. В печени синтезируются белки, выполняющие транспортные функции по отношению к витаминам. Например, ретинолсвязывающий белок (его содержание уменьшается при опухолях), витамин Е-связывающий белок и т.д. Часть витаминов, в первую очередь жирорастворимых, а также продуктов их преобразований выделяется из организма в составе жёлчи. 1.1.5 Участие печени в водно-минеральном обменеУчастие печени в водно-минеральном обмене состоит в том, что она дополняет деятельность почек в поддержании водно-солевого равновесия и является как бы внутренним фильтром, организма. Печень задерживает ионы Na+, К+, Сl-, Ca2+ и воду и выделяет их в кровь. Кроме того, печень депонирует макро- (К, Na, Ca, Mg, Fe) и микро- (Cu, Mn, Zn, Cо, As, Cd, Pb, Se) элементы и участвует в их распределении по другим тканям с помощью транспортных белков. Для накопления железа гепатоциты синтезируют специальный белок – ферритин. В ретикулоэндотелиоцитах печени и селезенки регистрируется водонерастворимый железосодержащий протеиновый комплекс – гемосидерин. В гепатоцитах синтезируется церулоплазмин, который, кроме вышеназванных функций, выполняет роль транспортного белка для ионов меди. Трансферрин, обладающий как и церулоплазмин, полифункциональностью, также образуется в печени и используется для переноса в плазме крови только ионов железа. Данный белок необходим для эмбрионального клеточного роста в период формирования печени. В печени ион Zn включается в алкогольдегидрогеназу, необходимую для биотрансформации этанола. Поступившие в гепатоциты соединения селена преобразуются в Se-содержащие аминокислоты и с помощью специфической т-РНК включаются в различные Se-протеины: глутатионпероксидазу (ГПО), 1-йодтиронин-5’-дейодиназу, Se-протеин Р. Последний считают основным транспортёром этого микроэлемента. Дейодиназа, обнаруженная не только в печени, обеспечивает конверсию прогормона тироксина в активную форму – трийодтиронин. Как известно, глутатионпероксидаза – ключевой фермент антирадикальной защиты. В печени сера, включённая в аминокислоты, окисляется до сульфатов, которые в виде ФАФС (фосфоаденозилфосфосульфатов) используются в реакциях сульфирования ГАГов, липидов, а также в процессах биотрансформации ксенобиотиков и некоторых эндогенных веществ (примеры продуктов инактивации – скатоксилсульфат, индоксилсульфат). Печень способна служить временным депо воды, особенно при отёках (количество Н2О может составлять до 80 % от массы органа) [6]. 1.1.6 Участие печени в пигментном обменеУчастие печени в обмене пигментов проявляется в превращении хромопротеидов до билирубина в клетках РЭС, имеющихся в печени, конъюгации билирубина в самих печеночных клетках и разложении в них всасывающегося из кишечника уробилиногена до непигментных продуктов. Гемохромогенные пигменты, образуются в организме при распаде гемоглобина (в значительно меньшей степени при распаде миоглобина, цитохромов и др.). Начальным этапом распада гемоглобина (в клетках макрофагов, в частности в звездчатых ретикулоэндотелиоцитах, а также в гистиоцитах соединительной ткани любого органа) является разрыв одного метинового мостика с образованием вердоглобина. В дальнейшем от молекулы вердоглобина отщепляются атом железа и белок глобин. В результате образуется биливердин, который представляет собой цепочку из четырех пиррольных колец, связанных метановыми мостиками. Затем биливердин, восстанавливаясь, превращается в билирубин – пигмент, выделяемый с желчью и поэтому называемый желчным пигментом. Образовавшийся билирубин называется непрямым (неконъюгированным) билирубином. Он нерастворим в воде, дает непрямую реакцию с диазореактивом, т.е. реакция протекает только после предварительной обработки спиртом. В печени билирубин соединяется (конъюгирует) с глюкуроновой кислотой. Эта реакция катализируется ферментом УДФ-глюкуронилтрансферазой, при этом глюкуроновая кислота вступает в реакцию в активной форме, т.е. в виде УДФГК. Образующийся глюкуронид билирубина получил название прямого билирубина (конъюгированный билирубин). Он растворим в воде и дает прямую реакцию с диазореактивом. Большая часть билирубина соединяется с двумя молекулами глюкуроновой кислоты, образуя диглюкуронид билирубина. Образовавшийся в печени прямой билирубин вместе с очень небольшой частью непрямого билирубина выводится с желчью в тонкую кишку. Здесь от прямого билирубина отщепляется глюкуроновая кислота и происходит его восстановление с последовательным образованием мезобилирубина и мезобилиногена (уробилиногена). Из тонкой кишки часть образовавшегося мезобилиногена (уробилиногена) резорбируется через кишечную стенку, попадает в воротную вену и током крови переносится в печень, где расщепляется полностью до ди- и трипирролов. Таким образом, в норме в общий круг кровообращения и мочу мезобилиноген не попадает. Основное количество мезобилиногена из тонкой кишки поступает в толстую и здесь восстанавливается до стеркобилиногена при участии анаэробной микрофлоры. Образовавшийся стеркобилиноген в нижних отделах толстой кишки (в основном в прямой кишке) окисляется до стеркобилина и выделяется с калом. Лишь небольшая часть стеркобилиногена всасывается в систему нижней полой вены (попадает сначала в геморроидальные вены) и в дальнейшем выводится с мочой (приложение 18). |
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.