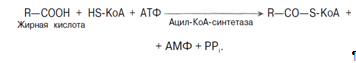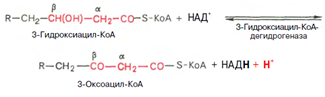|
|
МЕНЮ
|
Курсовая работа: Анализ биохимических показателей работы печени в норме и патологии
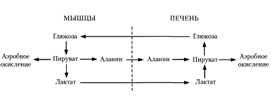
Из клеток, в которых происходит гликолиз, образующаяся молочная кислота поступает в кровь и улавливается в основном печенью, где и превращается в пируват. Пируват в печени частично окисляется, частично превращается в глюкозу — цикл Кори, или глюкозолактатпый цикл:
В организме взрослого человека за сутки может синтезироваться около 80 г глюкозы, главным образом в печени. Биологическое значение глюконеогенеза заключается не только в возвращении лактата в метаболический фонд углеводов, но и в обеспечении глюкозой мозга при недостатке углеводов в организме, например, при углеводном или полном голодании [2]. Синтез гликогена (гликогенез). Как уже говорилось выше, часть глюкозы поступившей в печень используется в синтезе гликогена. Гликоген — разветвленный гомополимер глюкозы, в котором остатки глюкозы соединены в линейных участках a-1,4-гликозидной связью. В точках ветвления мономеры соединены a-1,6-гликозидными связями. Эти связи образуются примерно с каждым десятым остатком глюкозы. Так возникает древообразная структура с молекулярной массой >107Д, что соответствует приблизительно 50 000 остатков глюкозы (приложение 9). При полимеризации глюкозы снижается растворимость образующейся молекулы гликогена и, следовательно, ее влияние на осмотическое давление в клетке. Это обстоятельство объясняет, почему в клетке депонируется гликоген, а не свободная глюкоза. Гликоген хранится в цитозоле клетки в форме гранул диаметром 10—40 нм. После приёма пищи, богатой углеводами, запас гликогена в печени может составлять примерно 5% от её массы. Распад гликогена печени служит в основном для поддержания уровня глюкозы в крови в постабсорбтивном периоде. Поэтому содержание гликогена в печени изменяется в зависимости от ритма питания. При длительном голодании оно снижается почти до нуля. Гликоген синтезируется в период пищеварения (через 1—2 ч после приёма углеводной пищи). Синтез гликогена из глюкозы требует затрат энергии. Прежде всего глюкоза подвергается фосфорилированию при участии фермента гексокиназы и глюкокиназы. Далее глюкозо-6-фосфат под влиянием фермента фосфоглюкомутазы переходит в глюкозо-1-фосфат. Образовавшийся глюкозо-1-фосфат уже непосредственно вовлекается в синтез гликогена. На первой стадии синтеза глюкозо-1-фосфат вступает во взаимодействие с УТФ (уридинтрифосфат), образуя уридиндифосфатглюкозу (УДФ-глюкоза) и пирофосфат. Данная реакция катализируется ферментом глюкозо-1-фосфат-уридилилтрансферазой (УДФГ-пирофосфорилаза) (приложение 10). На второй стадии — стадии образования гликогена — происходит перенос глюкозного остатка, входящего в состав УДФ-глюкозы, на глюкозидную цепь гликогена («затравочное» количество) (приложение 11). При этом образуется б-1,4-гликозидная связь между первым атомом углерода добавляемого остатка глюкозы и 4-гидроксильной группой остатка глюкозы цепи. Эта реакция катализируется ферментом гликогенсинтазой. Образующийся УДФ затем вновь фосфорилируется в УТФ за счет АТФ, и таким образом весь цикл превращений глюкозо-1-фосфата начинается сначала. Установлено, что гликогенсинтаза неспособна катализировать образование б-1,6-гликозидную связь, имеющуюся в точках ветвления гликогена. Этот процесс катализирует специальный фермент, получивший название гликогенветвящего фермента, или амило-1,4-1,6-трансглюкозидазы. Последний катализирует перенос концевого олигосахаридного фрагмента, состоящего из 6 или 7 остатков глюкозы, с нередуцирующего конца одной из боковых цепей, насчитывающей не менее 11 остатков, на 6-гидроксиль-ную группу остатка глюкозы той же или другой цепи гликогена. В результате образуется новая боковая цепь. Ветвление увеличивает скорость синтеза и расщепления гликогена [2]. Распад гликогена или его мобилизация происходят в ответ на повышение потребности организма в глюкозе. Гликоген печени распадается в основном в интервалах между приёмами пищи, распад ускоряется во время физической работы. Распад гликогена происходит при участии двух ферментов: гликогенфосфорилазы и фермента с двойной специфичностью — 4:4-трансферазы-б-1,6-гликозидазы. Гликогенфосфорилаза катализирует фосфоролиз 1,4-гликозидной связи нередуцирующих концов гликогена, глюкозные остатки отщепляются один за другим в форме глюкозо-1-фосфата (приложение 12). При этом гликогенфосфорилаза не может отщеплять глюкозные остатки от коротких ветвей, содержащих менее пяти глюкозных остатков; такие ветви удаляются 4:4-трансферазой-б-1,6-гликозидазой. Этот фермент катализирует перенос фрагмента из трех остатков короткой ветви на концевой глюкозный остаток более длинной ветви; кроме того, он гидролизует 1,6-гликозидную связь и таким образом удаляет последний остаток ветви (приложение 13). Голодание в течение 24 ч приводит практически к полному исчезновению гликогена в клетках печени. Однако при ритмичном питании каждая молекула гликогена может существовать неопределенно долго: при отсутствии пищеварения и поступления в ткани глюкозы молекулы гликогена уменьшаются за счет расщепления периферических ветвей, а после очередного приема пищи вновь вырастают до прежних размеров. Глюкозо-1-фосфат, образующийся из гликогена, при участии фосфоглюкомутазы превращается в глюкозо-6-фосфат, дальнейшая судьба которого в печени и в мышцах различна. В печени глюкозо-6-фосфат превращается в глюкозу при участии глюкозо-6-фосфатазы, глюкоза выходит в кровь и используется в других органах и тканях. Регуляция процессов гликогенеза и гликогенолиза осуществляется гормонами: инсулином, глюкагоном, адреналином. Первичный сигнал для синтеза инсулина и глюкагона — изменение концентрации глюкозы в крови. Инсулин и глюкагон постоянно присутствуют в крови, но при смене абсорбтивного периода на постабсорбтивный изменяется их относительная концентрация, что является главным фактором, переключающим метаболизм гликогена в печени. Отношение концентрации инсулина в крови к концентрации глюкагона называют «инсулин-глюкагоновый индекс». В постабсорбтивном периоде инсулин-глюкагоновый индекс снижается, и решающее значение в регуляции концентрации глюкозы и крови приобретает концентрация глюкагона. В период пищеварения преобладает влияние инсулина, так как инсулин-глюкагоновый индекс в этом случае повышается. В целом инсулин влияет на обмен гликогена противоположно глюкагону. Инсулин снижает концентрацию глюкозы в крови в период пищеварения. Гормон адреналин стимулирует выведение глюкозы из печени в кровь, для того чтобы снабдить ткани (в основном мозг и мышцы) «топливом» в экстремальной ситуации. Регуляторным фактором в метаболизме гликогена является также величина Км глюкокиназы, которая много выше, чем Км гексокиназы - печень не должна потреблять глюкозу для синтеза гликогена, если её количество в крови в пределах нормы. 1.1.2 Регуляция липидного обмена Липидный обмен в печени включает биосинтез различных липидов (холестерина, триацилглицерина, фосфоглицеридов, сфингомиелина и др.) которые поступают в кровь и распределяются по другим тканям и сгорание (окисление) жирных кислот с образованием кетоновых тел, которые используются как источник энергии для внепеченочных тканей. Доставка жирных кислот к месту окисления – к митохондриям клеток печени – происходит сложным путем: при участии альбумина осуществляется транспорт жирных кислот в клетку; при участии специальных белков – транспорт в пределах цитозоля; при участии карнитина – транспорт жирной кислоты из цитозоля в митохондрии. Процесс окисления жирных кислот складывается из следующих основных этапов. 1. Активация жирных кислот. Активация протекает на наружной поверхности мембраны митохондрии при участии АТФ, коэнзима А (HS-KoA) и ионов Mg2+. Реакция катализируется ферментом ацил-КоА-синтетазой:
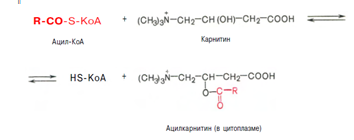
Активация протекает в 2 этапа. Сначала жирная кислота реагирует с АТФ с образованием ациладенилата, далее сульфгидрильная группа КоА действует на прочно связанный с ферментом ациладенилат с образованием ацил-КоА и АМФ. Затем следует транспорт жирных кислот внутрь митохондрий. Переносчиком активированных жирных кислот с длинной цепью через внутреннюю митохондриальную мембрану служит карнитин. Ацильная группа переносится с атома серы КоА на гидроксильную группу карнитина. 2. Образуется ацилкарнитин, который диффундирует через внутреннюю митохондриальную мембрану:
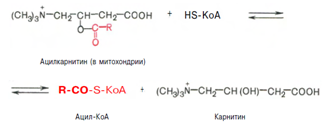
Реакция протекает при участии спецефического цитоплазматического фермента карнитин-ацилтрансферазы. После прохождения ацилкарнитина через мембрану митохондрий происходит обратная реакция – расщепление ацилкарнитина при участии HS-KoA и митохондриальной карнитин-ацилтрансферазы:
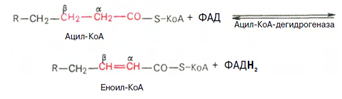
3. Внутримитохондриальное окисление жирных кислот. Процесс окисления жирной кислоты в митохондриях клетки включает несколько последовательных реакций. Первая стадия дегидрирования. Ацил-КоА в митохондриях подвергается ферментативному дегидрированию, при этом ацил-КоА теряет 2 атома водорода в б- и в-положениях, превращаясь в КоА-эфир ненасыщенной кислоты. Реакцию катализирует ацил-КоА-дегидрогеназа, продуктом является еноил-КоА :
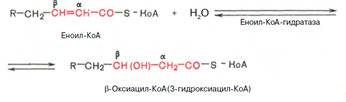
Стадия гидратации. Ненасыщенный ацил-КоА (еноил-КоА) при участии фермента еноил-КоА-гидратазы присоединяет молекулу воды. В результате образуется в-оксиацил-КоА (или 3-гидроксиацил-КоА):
Вторая стадия дегидрирования. Образовавшийся в-оксиацил-КоА (3-гидроксиацил-КоА) затем дегидрируется. Эту реакцию катализируют НАД-зависимые дегидрогеназы:
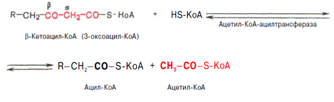
Тиолазная реакция. Расщепление 3-оксоацил-КоА с помощью тиоловой группы второй молекулы КоА. В результате образуется укороченный на два углеродных атома ацил-КоА и двууглеродный фрагмент в виде ацетил-КоА. Данная реакция катализируется ацетил-КоА-ацилтрансферазой (в-ке-тотиолазой):
Образовавшийся ацетил-КоА подвергается окислению в цикле трикарбоновых кислот, а ацил-КоА, укоротившийся на два углеродных атома, снова многократно проходит весь путь в-окисления вплоть до образования бутирил-КоА (4-углеродное соединение), который в свою очередь окисляется до 2 молекул ацетил-КоА [2]. Биосинтез жирных кислот. Синтез жирных кислот протекает в цитоплазме клетки. В митохондриях в основном происходит удлинение существующих цепей жирных кислот. Установлено, что в цитоплазме печеночных клеток синтезируется пальмитиновая кислота (16 углеродных атомов), а в митохондриях этих клеток из этой пальмитиновой кислоты или из жирных кислот экзогенного происхождения, т.е. поступающих из кишечника, образуются жирные кислоты, содержащие 18, 20 и 22 углеродных атома. Митохондриальная система биосинтеза жирных кислот, включает несколько модифицированную последовательность реакций в-окисления, и осуществляет только удлинение существующих в организме среднецепочечных жирных кислот, в то время как полный биосинтез пальмитиновой кислоты из ацетил-КоА активно протекает в цитозоле, т.е. вне митохондрий, по совершенно другому пути. Внемитохондриальная система биосинтеза жирных кислот (липогенез) находится в растворимой (цитозольной) фракции клеток печени. Биосинтез жирных кислот протекает с участием НАДФН, АТФ, Мn2+ и НСО3– (в качестве источника СО2); субстратом является ацетил-КоА, конечным продуктом – пальмитиновая кислота. Образование ненасыщенных жирных кислот. Элонгация жирных кислот. Две наиболее распространенные мононенасыщенные жирные кислоты – пальмитоолеиновая и олеиновая – синтезируются из пальмитиновой и стеариновой кислот. Эти превращения протекают в микросомах клеток печени. Превращению подвергаются только активированные формы пальмитиновой и стеариновой кислот. Ферменты, участвующие в этих превращениях, получили название десатураз. Наряду с десатурацией жирных кислот (образование двойных связей) в микросомах происходит и их удлинение (элонгация), причем оба эти процесса могут сочетаться и повторяться. Удлинение цепи жирной кислоты происходит путем последовательного присоединения к соответствующему ацил-КоА двууглеродных фрагментов при участии малонил-КоА и НАДФН. Ферментная система, катализирующая удлинение жирных кислот, получила название элонгазы. Пути превращения пальмитиновой кислоты в реакциях десатурации и элонгации представлены в приложении 14. Биосинтез триглицеридов. Синтез триглицеридов происходит из глицерина и жирных кислот (главным образом стеариновой, пальмитиновой и олеиновой). Первый путь биосинтеза триглицеридов в печени протекает через образование б-глицерофосфата (глицерол-3-фосфата) как промежуточного соединения, глицерин фосфорилируется за счет АТФ с образованием глицерол-3-фосфата:
Второй путь в основном связан с процессами гликолиза и гликогенолиза. Известно, что в процессе гликолитического распада глюкозы образуется дигидроксиацетонфосфат, который в присутствии цитоплазматической глицерол-3-фосфатдегидрогеназы способен превращаться в глицерол-3-фосфат:
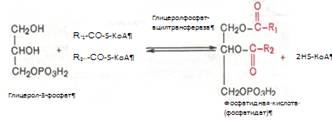
Образовавшийся тем или иным путем глицерол-3-фосфат последовательно ацилируется двумя молекулами КоА-производного жирной кислоты. В результате образуется фосфатидная кислота (фосфатидат):
Ацилирование глицерол-3-фосфата протекает последовательно, т.е. в 2 этапа. Сначала глицерол-3-фосфат-ацилтрансфераза катализирует образование лизофосфатидата. Далее фосфатидная кислота гидролизуется фосфатидат-фосфогидролазой до 1,2-диглицерида (1,2-диацилглицерола):
Затем 1,2-диглицерид ацилируется третьей молекулой ацил-КоА и превращается в триглицерид (триацилглицерол). Эта реакция катализируется диацилглицерол-ацилтрансферазой:
Установлено, что большинство ферментов, участвующих в биосинтезе триглицеридов, находятся в эндоплазматическом ретикулуме, и только некоторые, например глицерол-3-фосфат-ацилтрансфераза,– в митохондриях. Метаболизм фосфолипидов. Фосфолипиды играют важную роль в структуре и функции клеточных мембран, активации мембранных и лизосомальных ферментов, в проведении нервных импульсов, свертывании крови, иммунологических реакциях, процессах клеточной пролиферации и регенерации тканей, в переносе электронов в цепи дыхательных ферментов. Особая роль фосфолипидам отводится в формировании липопротеидных комплексов. Наиболее важные фосфолипиды синтезируются главным образом в эндоплазматической сети клетки. Центральную роль в биосинтезе фосфолипидов играют 1,2-диглицериды (в синтезе фосфатидилхолинов и фосфатидилэтаноламинов), фосфатидная кислота (в синтезе фосфатидилинозитов) и сфингозин (в синтезе сфингомиелинов). Цитидинтрифосфат (ЦТФ) участвует в синтезе практически всех фосфолипидов. Биосинтез холестерина. В синтезе холестерина можно выделить три основные стадии: I – превращение активного ацетата в мевалоновую кислоту, II – образование сквалена из мевалоновой кислоты, III – циклизация сквалена в холестерин. Рассмотрим стадию превращения активного ацетата в мевалоновую кислоту. Начальным этапом синтеза мевалоновой кислоты из ацетил-КоА является образование ацетоацетил-КоА посредством обратимой тиолазной реакции. Затем при последующей конденсации ацетоацетил-КоА с 3-й молекулой ацетил-КоА при участии гидроксиметилглутарил-КоА-синтазы (ГМГ-КоА-синтаза) образуется в-гидрокси-в-метилглутарил-КоА. Далее в-гидрокси-в-метилглутарил-КоА под действием регуляторного фермента НАДФ-зависимой гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоА-редуктаза) в результате восстановления одной из карбоксильных групп и отщепления HS-KoA превращается в мевалоновую кислоту. Наряду с классическим путем биосинтеза мевалоновой кислоты имеется второй путь, в котором в качестве промежуточного субстрата образуется в-гидрокси-в-метилглутарил-S-АПБ. Реакции этого пути идентичны начальным стадиям биосинтеза жирных кислот вплоть до образования ацетоацетил-S-АПБ. В образовании мевалоновой кислоты по этому пути принимает участие ацетил-КоА-карбоксилаза – фермент, осуществляющий превращение ацетил-КоА в малонил-КоА. На II стадии синтеза холестерина мевалоновая кислота превращается в сквален. Реакции II стадии начинаются с фосфорилирования мевалоновой кислоты с помощью АТФ. В результате образуется 5-фосфорный эфир, а затем 5-пирофосфорный эфир мевалоновой кислоты 5-пирофосфомевалоновая кислота в результате последующего фосфорилирования третичной гидроксильной группы образует нестабильный промежуточный продукт – 3-фосфо-5-пирофосфомевалоновую кислоту, которая, декарбоксилируясь и теряя остаток фосфорной кислоты, превращается в изопентенилпирофосфат. Последний изомеризуется в диметил-аллилпирофосфат. Затем оба изомерных изопентенилпирофосфата (диметилаллилпирофосфат и изопентенилпирофосфат) конденсируются с высвобождением пирофосфата и образованием геранилпирофосфата. К геранилпирофосфату вновь присоединяется изопентенилпирофосфат. В результате этой реакции образуется фарнезилпирофосфат. В заключительной реакции данной стадии в результате НАДФН-зависимой восстановительной конденсации 2 молекул фарнезилпирофосфата образуется сквален. На III стадии биосинтеза холестерина сквален под влиянием сквален-оксидоциклазы циклизируется с образованием ланостерина. Дальнейший процесс превращения ланостерина в холестерин включает ряд реакций, сопровождающихся удалением трех метильных групп, насыщением двойной связи в боковой цепи и перемещением двойной связи. Общая схема синтеза холестерина представлена в приложении 15. Метаболизм кетоновых тел. Под термином кетоновые (ацетоновые) тела подразумевают ацетоуксусную кислоту (ацетоацетат) СН3СОСН2СООН, в-оксимасляную кислоту (в-оксибутират, или D-3-гидроксибутират) СН3СНОНСН2СООН и ацетон СН3СОСН3. |
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.